
内酰胺类化合物是一类具有重要应用价值的氮杂环骨架单元,广泛存在于生物活性分子及天然产物当中。尤其对于含有烯烃的内酰胺,结构应用广泛且化学转化丰富。近年来,此类化合物的合成方法得到了快速发展,但以高效且多样化的方式从市售原料快速地构建多官能团的内酰胺,如含有碳碳双键的 γ-和 δ-内酰胺仍然具有挑战性。
近日,我院钱鹏程-李龙教授课题组实现了烯烃取代内酰胺的高效、多样性合成。该方法研究了在锌催化剂作用下,烯炔酰胺化合物的分子间氧化环化反应。这种廉价金属催化的氧化环化反应具有高产率和优异的区域选择性、立体选择性等优点。
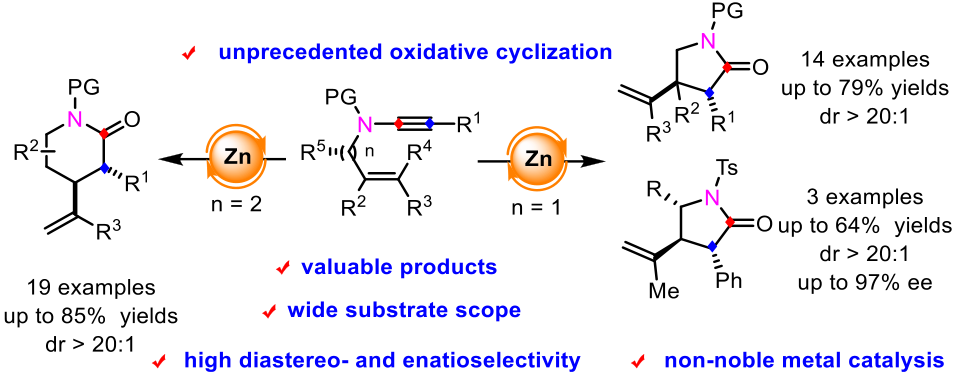
首先,作者选择1,5-烯炔酰胺作为模型底物进行了一系列条件筛选,最终发现以2,6-二溴吡啶氮氧化合物作为氧化剂,并添加4 Å 分子筛作为除水剂,在三氟甲烷磺酸锌的催化作用下,于80 ℃的氯苯中反应1 h,并于反应结束后添加碳酸铯继续搅拌2 h,可以79%的产率、大于20/1的dr值得到目标 γ-内酰胺化合物。随后,作者在最优条件下对反应的官能团耐受性进行了考察。炔酰胺上无论引入供电子基团或吸电子基团,反应仍能保持中等至良好的收率;令人高兴的是,杂环取代的炔酰胺也适用于该反应。紧接着,作者探索了1,6-烯炔酰胺作为底物的反应情况,亦可高效、高非对映选择性地得到目标 δ-内酰胺化合物。此外,获得的 γ-内酰胺化合物可以通过一系列适当的转化构建其他五元氮杂环化合物,其中包括PKA/PKAB3活性抑制剂的类似物,有望应用于医药化学品领域。
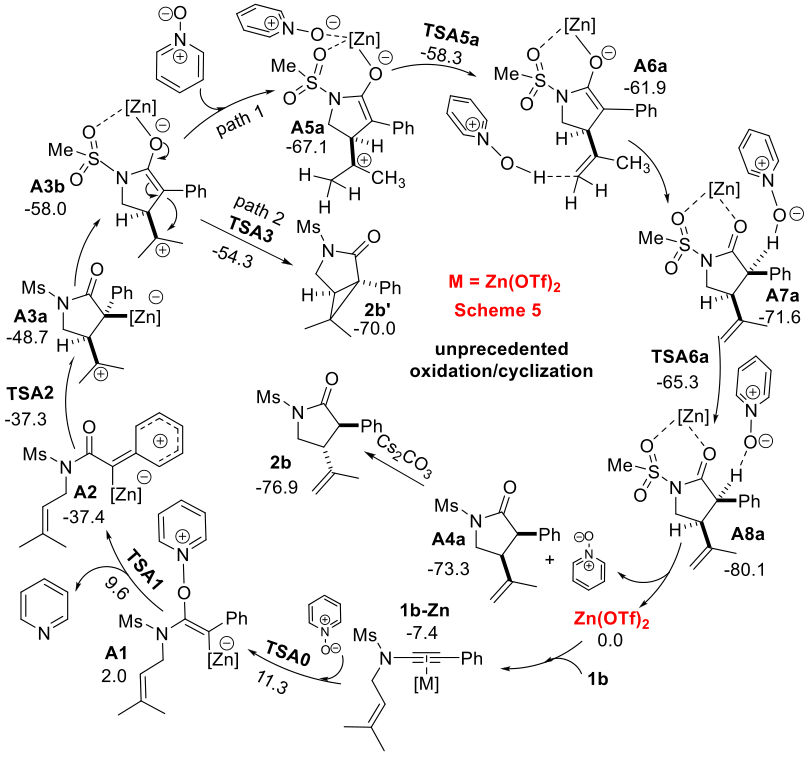
根据以上实验结果并结合理论计算研究(南京农业大学邓超副教授合作),作者提出了一种可能的机理:首先炔酰胺被金属催化剂三氟甲烷磺酸锌活化,炔酰胺受分子间氮氧氧化生成烯基金属中间体A1;紧接着,苯环上的π电子反馈回来,促进了分子内的类烯醇互变反应得到酰胺金属中间体A2;随后,该中间体被分子内的烯烃捕获生成异丙基正离子中间体A3a;最后发生金属迁移/烯醇互变/氢消除反应,得到顺反两种构型的 γ-内酰胺化合物,此时,再添加碳酸铯搅拌2 h后可使产物转化为热力学稳定的反式构型 γ-内酰胺化合物。
相关科研成果发表于近期的《Organic Letters》(DOI: 10.1021/acs.orglett.2c02871),温州大学为第一通讯单位,我院博士后朱伯汉为第一作者,相关工作受到国家自然科学基金项目(No. 21828102)、温州市科技局基金项目(No. ZY2020027)和厦门大学固体表面物理化学国家重点实验室(202004)等的支持。
原文链接: