作者:Meng-Qiang Zeng; Ke-Xin Feng; Bo-Lun Hu; Hai-Yong Tu and Xing-Guo Zhang.
论文题目:Ni-Catalyzed Reductive Arylalkenylation of Alkynes for the Selective Synthesis of Polysubstituted Naphthalenes.
DOI:10.1021/acs.orglett.2c02068
//doi.org/10.1021/acs.orglett.2c02068

多取代萘是一类重要的芳香族化合物,有着独特的生物活性,是许多医药、农药的中间体。最近,硕士研究生曾猛强等人在张兴国教授和涂海勇副教授的指导下发展了一种高效安全的合成2-三氟甲基萘和萘甲酸乙酯的新方法。该方法研究了在锌粉存在下,镍催化1-溴-2-(2-氯乙烯基)芳烃与炔烃的还原芳基烯基化反应。这种无碱环化策略具有良好的产率和优秀的官能团耐受性等优点。相关结果发表在Organic Letters。

首先,作者选择2-氯-1-(2-溴苯)-3、3、3-三氟丙烯(1a)与苯乙炔(2a)反应作为模型反应,对反应条件进行了探究。结果显示,以碘化镍为催化剂,2,2-联吡啶-4,4-甲酸甲酯为配体,锌粉为还原剂,N-甲基-2-吡咯烷酮为溶剂,反应温度为80 ℃,在氮气氛围下反应12小时,获得了最高收率为84%。随后,作者在最优条件下对反应的官能团容忍性进行了考察,苯乙炔上无论引入供电子基团或是吸电子基团时,反应仍保持中等至优良的收率。采用对称或不对称内炔也可以获得较优的收率,同时杂环炔也是合适的底物。底物2-氯-1-(2-溴苯)-3、3、3-三氟丙烯的芳环上引入供电子基团或是吸电子基团时,反应仍保持优良的收率。把底物1a换作乙基-3-(2-溴苯基)-2-氯丙烯酸酯也可以顺利地用于这个还原芳基烯基化反应,并获得中等的收率。此外,衍生自药物(如雌酮和布洛芬等)的末端炔烃也能顺利发生反应,以较优的产率得到相应的目标产物。
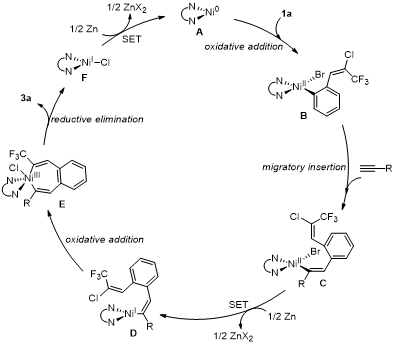
根据以上实验结果,作者提出了一下的可能机理:首先,1a与Ni(0)物种A氧化加成生成芳基镍中间体B,经过迁移插入过程形成乙烯基-NiII-Br。随后,中间体C与Zn的单电子还原得到乙烯基-NiI中间体D,随后与烯基氯发生分子内氧化加成得到Ni(III)物种E。然后,中间体E参与还原消除生成产物3a和Ni(I)物种F。最后,Ni(I)物种F被锌还原生成Ni(0)以关闭催化循环。